Bio-Share | TCE 加速进入临床应用:结构创新、效力提升与 CMC 平台的关键作用
发布时间: Dec 05 , 2025
双特异性抗体在癌症免疫治疗中的最早探索,主要集中在“引导” T 细胞去精准识别并杀伤肿瘤细胞。T 细胞募集型双抗(TCE)正是基于这一思路诞生的,它通过一端结合肿瘤细胞(肿瘤相关抗原,TAA),另一端结合 T 细胞上的 CD3(通常为 CD3ε),从而在两者之间搭建起高效的免疫突触,直接触发 T 细胞的定向攻击。由于 TCE 的作用机制不依赖于主要组织相容性复合体(MHC),它能够在不同 MHC 背景的患者中发挥作用,并有效规避免疫系统常见的肿瘤逃逸方式,例如 MHC 缺失或抗原呈递通路受损[1]。这种利用双抗重定向 T 细胞的思路,最早在上世纪 80 年代中期就已被证明可行[2]。
2009 年,Catumaxomab(卡妥索单抗)成为全球首个获批用于临床的 T 细胞募集型双抗(TCE)。这是一款由小鼠和大鼠抗体杂交而成的双特异性 IgG,能够同时结合肿瘤细胞上的 EpCAM 以及 T 细胞上的 CD3ε,最初用于腹腔内给药治疗恶性腹水,可有效清除肿瘤细胞。
然而,随着临床使用的推进,Catumaxomab 会引发明显的免疫相关毒性。其带有活性的 Fc 结构域会与体内表达 Fcγ 受体的免疫细胞发生非特异性结合,引发强烈的细胞因子释放综合征(CRS)和 T 细胞介导的肝毒性。这些安全性问题最终限制了它的应用范围。由于商业和安全性方面的因素,Catumaxomab 于2017年在欧洲被撤回。尽管如此,它作为首个用于临床的 T 细胞募集型双特异性抗体,在 TCE 领域具有代表性。
Blinatumomab(贝林妥欧单抗,商品名 BLINCYTO®)是一款针对 B 细胞表面 CD19 的双特异性 T 细胞连接抗体(BiTE™),并于 2014 年获批上市,成为 TCE 领域的关键里程碑。自此之后,围绕血液肿瘤和实体瘤中不同肿瘤相关抗原(TAA)开展 TCE 药物开发的兴趣迅速升温,各类新靶点和新结构不断涌现。
BiTE™(Bispecific T-cell Engager)是一类典型的 T 细胞募集型双特异性抗体,其结构由两个串联的单链可变片段(scFv)组成,通过短柔性 Linker 相连,一端识别肿瘤相关抗原(TAA),另一端结合 T 细胞表面的 CD3。该构型具备分子量小、构象灵活、易于促进免疫突触形成等特点,能够高效介导 T 细胞对肿瘤细胞的定向杀伤。然而,由于其缺乏 Fc 区域,BiTE 在体内清除迅速,半衰期较短,通常需要持续输注,这也成为推动后续长效化工程(如 Fc 融合、白蛋白结合域引入、PEG 化)发展的重要原因。
影响 TCE 治疗效力和安全性的因素有很多,因此在早期设计层面,会考量诸多因素,例如上面提到 BiTE™,小而灵活的结构可以提高突触形成的效率,但却无法避免频繁给药。除了分子大小的影响外,T 细胞和肿瘤细胞之间的突触距离同样至关重要,这一因素直接影响 T 细胞的活化效率和肿瘤细胞的杀伤能力。Austin 等人已经表明,为了形成有效的免疫突触,T 细胞与抗原呈递细胞之间的最佳膜间距离约为 15nm[3]。同时抗 TAA 和抗 CD3 臂靠得更近的 TCE 构型显示出增强的 T 细胞活化和优异的肿瘤细胞杀伤[4]。相反,随着 TCE 两个结合域之间的间隔增加,其整体效力往往会下降。
除了空间结构之外,亲和力与价数的调控同样是 TCE 优化的重要环节。在 TCE 分子中引入多个 TAA 结合结构域,TCE 可获得更高的多价结合能力,从而提升杀伤效应,并在低表达或高度异质的肿瘤环境中保持活性。此外,双价 TAA 结合还能允许单个结合臂具较低亲和力[5],减少与可溶性抗原结合造成的“抗原汇效应”。
2+1 结构的 TCE(两个 TAAFab + 一个 CD3Fab)在临床前和临床中均显示出良好的抗肿瘤活性,如 Glofitamab(COLUMVI™, Roche)[6-8]:靶向 CD20,和 Xaluritamig(Amgen)[9]:靶向 STEAP1。有些团队还尝试用 IgM 五聚体/六聚体来做双抗[10],通过更多结合位点提升整体“抓力”。但这些更大的分子在临床上显示的效力还不算理想。因此价数(valency)的优化需要在“高效结合”与“保持良好肿瘤渗透与效力”之间取得平衡。
CD3 是由 CD3ε、CD3δ、CD3γ 和 CD3ζ 链组成的多亚基复合物,与 TCR(T细胞受体)相关。不同抗体结合 CD3ε 的不同表位会触发强弱不同的 TCR 信号,从而影响 T 细胞杀伤与细胞因子释放的比例,进而影响 CRS 风险。早期的 TCE 多采用高亲和力 CD3 结合臂,虽然能强效杀伤肿瘤,但也容易引起 T 细胞过度激活,导致严重 CRS。随着研究深入,人们发现“杀伤作用阈值低于细胞因子释放阈值”,也就是说,T 细胞并不需要非常强的激活信号就能完成杀伤。因此,降低 CD3 亲和力成为新一代 TCE 的关键设计方向:弱亲和力 CD3 既能保持肿瘤杀伤效应,又能显著减少细胞因子释放[5]。
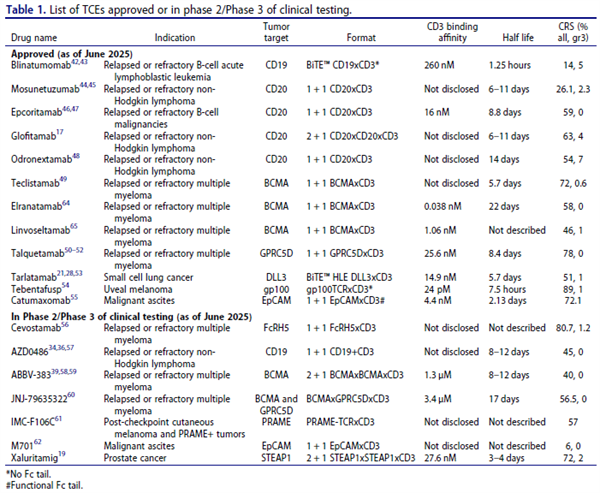
表1: 正在进行临床试验的 TCEs
下一代 TCEs 旨在提高肿瘤细胞杀伤,提高精确度和安全性,并减轻耐药性的发展,这是单一疗法治疗的常见问题(图1)。然而,临床挑战依然存在。目前,减少 TCE 诱发 CRS 的主要策略仍是通过可控给药方案(如引导剂量 priming dose、阶梯递增剂量 step-up dose、以及皮下注射制剂)来缓解初始细胞因子激增,并帮助患者逐步获得耐受。这些给药策略能够调节 TCE 的暴露量和药效学特征,从而改善安全性。
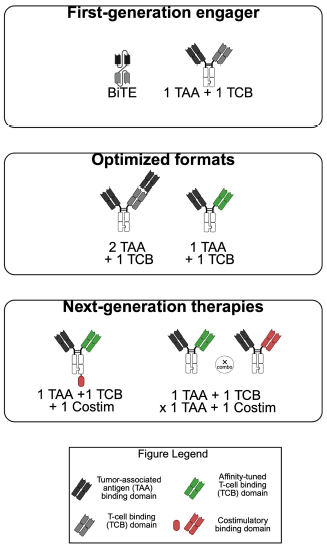
图1:TCE 结构格式从 BiTE 到下一代工程化设计的升级路线图
更安全、治疗窗口更大的 TCE 将为与免疫检查点抑制剂、细胞因子疗法、TKI、ADC 等多种方案的联合治疗创造更大空间,从而在实体瘤中实现更灵活、更个体化的治疗策略。
随着多种新型 TCE 工程策略不断成熟(如CD3 亲和力调控、2+1 格式、多价结构等),双抗产品的分子结构日益复杂,对CMC 体系也提出了更高要求。从高表达细胞株、非对称结构正确配对,到下游纯化策略、稳定性与杂质控制,再到 GMP 生产,CMC 能力已成为推动 TCE/双抗临床转化的关键环节。
康日百奥Bioworkshops 已经建立了成熟的#多特异性抗体开发平台,专注于#复杂抗体开发,平台覆盖双抗、#三抗 等复杂抗体开发的全流程服务:
1、多样化#分子设计 支持:覆盖对称型、非对称型、IgG-like等多种抗体分子结构,能够在项目早期提供分子设计评估与技术支持,助力高效推进后续工艺开发;
2、#高表达系统:优化质粒构建与转染策略,配合高产#稳定细胞株开发,显著提升抗体表达量与正确组装率;
3、完整#开发体系:从#分子设计评估、#细胞株开发、#工艺优化 到#GMP生产,全流程保障双抗等复杂抗体产品的质量与可放大性;
4、成熟项目经验:平台已成功交付多个临床阶段双抗项目,广泛覆盖#肿瘤免疫、#炎症 及#自身免疫 等治疗领域。
参考来源
[1] Garrido F. HLA class-I expression and cancer immunotherapy. Adv Exp Med Biol 2019;1151:79–90.
[2] Staerz UD, Kanagawa O, Bevan MJ. Hybrid antibodies can target sites for attack by T cells. Nature 1985;314:628–31.
[3] Austin RJ, Lemon BD, Aaron WH, Barath M, Culp PA, DuBridge RB, Evnin LB, Jones A, Panchal A, Patnaik P, et al. TriTACs, a novel class of T-Cell-engaging protein constructs designed for the treatment of solid tumors. Mol Cancer Ther. 2021;20(1):109–120.
[4] Leithner A, Staufer O, Mitra T, Liberta F, Valvo S, Kutuzov M, Dada H, Spaeth J, Zhou W, Schiele F, et al. Solution structure and synaptic analyses reveal determinants of bispecific T cell engager potency. Proc Nat Acad Sci. 2024;122(22):e2425781122.
[5] Cristina Bergamaschi, Miguel Gaspar, Thomas Ciucci, Suzanne I. Sitnikova, Corinne Cayatte, Mike Pica, Simon J. Dovedi. Innovative strategies for T cell engagers for cancer immunotherapy. mAbs. 2025;17(1):2531223.
[6] Bacac M, Colombetti S, Herter S, Sam J, Perro M, Chen S, Bianchi R, Richard M, Schoenle A, Nicolini V, et al. CD20-TCB with obinutuzumab pretreatment as next-generation treatment of hematologic malignancies. Clin Cancer Res. 2018;24(19):4785–4797.
[7] Hutchings M, Morschhauser F, Iacoboni G, Carlo-Stella C, Offner FC, Sureda A, Salles G, Martínez-Lopez J, Crump M, Thomas DN, et al. Glofitamab, a novel, bivalent CD20-targeting T-Cell-engaging bispecific antibody, induces durable complete remissions in relapsed or refractory B-Cell lymphoma: a phase I trial. J Clin Oncol. 2021;39(18):1959–1970.
[8] Dickinson MJ, Carlo-Stella C, Morschhauser F, Bachy E, Corradini P, Iacoboni G, Khan C, Wróbel T, Offner F, Trněný M, et al. Glofitamab for relapsed or refractory diffuse large B-Cell lymphoma. N Engl J Med. 2022;387 (24):2220–2231.
[9] Kelly WK, Danila DC, Lin CC, Lee J-L, Matsubara N, Ward PJ, Armstrong AJ, Pook D, Kim M, Dorff TB, et al. Xaluritamig, a STEAP1 x CD3 XmAb 2+1 immune therapy for metastatic castration-resistant prostate cancer: results from dose exploration in a first-in-human study. Cancer Discov. 2024;14(1):76–89.
[10] Kaveri SV, Silverman GJ, Bayry J. Natural IgM in immune equilibrium and harnessing their therapeutic potential. The J Immunol. 2012;188:939–945.
关于康日百奥Bioworkshops
康日百奥Bioworkshops 是一家全球化的生物药合同开发与生产组织(CDMO),专注于抗体类生物药的研发与生产。我们在双特异性、三特异性、融合蛋白等复杂抗体领域具备突出优势,为全球制药与生物技术公司提供从早期研发到商业化生产的一站式解决方案。依托完善的体系和国际标准合规的质量管理,康日百奥Bioworkshops 的服务范围覆盖细胞株构建、工艺开发、原液生产(200L、500L、2000L)、制剂灌装(西林瓶水针、冻干、预充针、卡式瓶等主流剂型,并支持与注射笔等给药装置的配套使用)、工艺表征,工艺验证以及注册申报支持。作为值得信赖的合作伙伴,康日百奥Bioworkshops 已经与来自美国、欧洲、亚太等地的客户开展合作,成功交付其单抗、双抗、多抗、ADC、融合蛋白、细胞因子等项目并获得临床批件。我们坚持以客户需求为中心,通过专业团队和先进平台,加速创新药物的开发和上市进程。
公司业务范围:
细胞株构建 | 细胞培养 | 纯化工艺开发 | 制剂处方开发 | 分析方法开发 | 工艺表征工艺验证 | 原液和成品的 cGMP 生产(200L、500L、2000L) | 无菌灌装(预充针、卡式瓶、注射笔、西林瓶水针、冻干)
















