Antibodies to Watch:2025年19款抗体新药全景盘点
发布时间: Mar 09 , 2026
在年度综述 《Antibodies to Watch in 2026》[1] 中,研究人员对全球抗体药物的研发与审批进展进行了系统盘点。数据显示,自2010年以来,全球进入临床后期阶段的抗体药物数量已从 26个增加到200多个。2025年,全球共有 19款抗体药物首次获批上市,同时仍有 26个候选药物处于监管审评阶段。
与此同时,全球抗体创新格局也在发生变化。过去抗体药物研发主要集中在欧美,但近年来 中国企业在该领域的影响力持续提升。2025年获批的抗体药物中,超过一半来自中国公司。
本文将结合该报告,对 2025年全球获批的19款抗体新药进行简单梳理,并看看其中反映出的 技术趋势和产业变化。
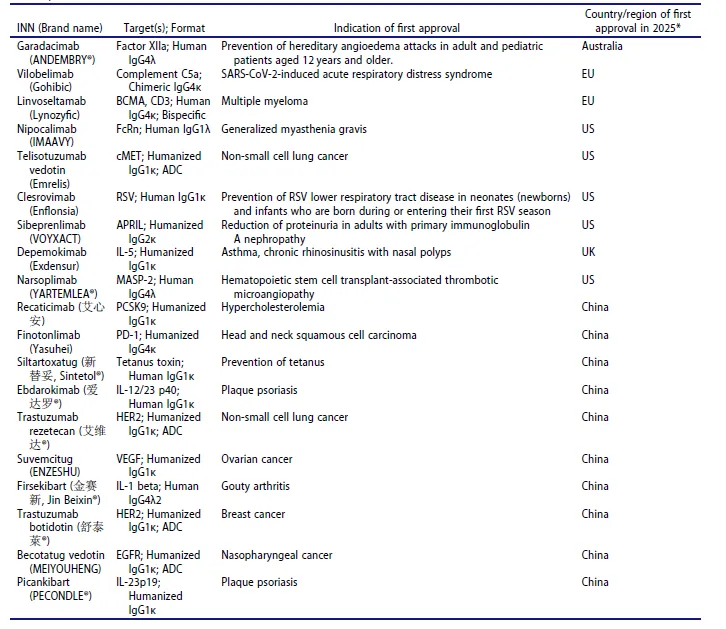
表1:2025年在全球任何国家首次获得上市批准的商业化单克隆抗体治疗药物
2025年全球获批的19款抗体新药
1 Garadacimab(CSL)
Garadacimab(ANDEMBRY®)[2]是一种靶向凝血因子XIIa(FXIIa)的IgG4单克隆抗体,用于预防遗传性血管性水肿(HAE)发作。该抗体通过抑制FXIIa的蛋白水解活性,从而阻断相关炎症及凝血通路。2025年1月,该药首先在澳大利亚获批,随后在英国、欧盟、日本、瑞士、美国和加拿大相继获批。
2 Vilobelimab(InflaRx)
Vilobelimab(Gohibic®)是一种嵌合IgG4κ抗体,靶向补体系统关键炎症介质C5a,用于治疗由SARS-CoV-2感染引起的急性呼吸窘迫综合征(ARDS)。2025年该药在欧盟获得附条件上市许可。临床研究显示,在接受机械通气的COVID-19重症患者中,vilobelimab联合标准治疗可显著降低28天全因死亡率。[3,4]
3 Linvoseltamab(Regeneron)
Linvoseltamab(Lynozyfic®)是一种双特异性抗体,同时靶向BCMA和CD3,通过激活T细胞杀伤多发性骨髓瘤细胞。2025年,该药在欧盟获得有条件上市批准,并在美国获得加速批准,用于既往接受多线治疗的复发或难治性多发性骨髓瘤患者。临床研究显示,该药具有持久的抗肿瘤反应。[5]
4 Nipocalimab(强生)
Nipocalimab(IMAAVY®)是一种靶向新生儿Fc受体(FcRn)的IgG1抗体,可阻断IgG循环回收,从而降低致病性自身抗体水平。2025年,美国FDA批准该药用于治疗抗AChR或MuSK抗体阳性的全身型重症肌无力患者。[6,7,8]
5 Telisotuzumab vedotin(AbbVie)
Telisotuzumab vedotin(Emrelis®)是一种靶向c-MET的抗体药物偶联物(ADC),通过抗体将细胞毒药物MMAE递送至肿瘤细胞。2025年,美国FDA加速批准该药用于治疗c-MET高表达的非小细胞肺癌。[9]
6 Clesrovimab(Merck)
Clesrovimab(Enflonsia®)是一种靶向呼吸道合胞病毒(RSV)F蛋白的人源IgG1抗体,并通过YTE突变延长半衰期。2025年,该药获得FDA批准,用于预防新生儿和婴幼儿RSV下呼吸道感染。[10,11]
7 Sibeprenlimab(大冢制药)
Sibeprenlimab(VOYXACT®)是一种靶向APRIL细胞因子的IgG2κ抗体,用于治疗IgA肾病。APRIL在异常IgA产生中发挥关键作用。2025年FDA加速批准该药用于减少IgA肾病患者蛋白尿水平。[12]
8 Depemokimab(GSK)
Depemokimab(Exdensur®)是一种靶向IL-5的长效抗体,用于治疗嗜酸性粒细胞型哮喘及鼻息肉相关慢性鼻窦炎。该抗体经过工程化改造具有超长半衰期,可实现每6个月给药一次。2025年,该药在英国获得批准,并随后在美国获批。[13,14]
9 Narsoplimab(Omeros)
Narsoplimab(YARTEMLEA®)是一种靶向MASP-2的IgG4λ抗体,通过抑制补体凝集素途径发挥作用。2025年FDA批准该药用于治疗造血干细胞移植相关血栓性微血管病(TA-TMA)。临床研究显示,该药可显著提高患者生存率。[15]
中国2025年首次获批抗体
10 Recaticimab(恒瑞医药)
Recaticimab(艾心安®)是一种靶向PCSK9的人源化IgG1κ抗体,用于治疗高胆固醇血症。该药通过阻断PCSK9与LDL受体结合,从而增加LDL-C清除。III期研究显示,该药可降低LDL-C约45%–60%,并具有较长半衰期。[16]
11 Finotonlimab(神州细胞)
Finotonlimab(安佑平®)是一种PD-1单克隆抗体,用于治疗复发或转移性头颈鳞癌。2025年中国批准该药联合化疗用于一线治疗。III期研究显示,该治疗方案可显著延长患者总体生存期。[17]
12 Siltartoxatug(泰诺麦博)
Siltartoxatug(新替妥®)是一种靶向破伤风毒素的IgG1抗体,用于破伤风暴露后的被动免疫预防。2025年中国优先审评批准该药上市。[18]
13 Ebdarokimab(康方生物)
Ebdarokimab(爱达罗®)是一种靶向IL-12/23 p40亚基的抗体,可抑制Th1和Th17炎症通路。2025年中国批准该药用于治疗中重度斑块型银屑病。临床研究显示,该药具有良好的疗效和长期安全性。[19]
14 Trastuzumab rezetecan(恒瑞医药)
Trastuzumab rezetecan(艾维达®)是一种靶向HER2的ADC,通过连接拓扑异构酶I抑制剂发挥抗肿瘤作用。2025年中国批准该药用于HER2突变的非小细胞肺癌。[20,21]
15 Suvemcitug(先声药业)
Suvemcitug(ENZESHU®)是一种靶向VEGF的人源化抗体,可抑制肿瘤血管生成。2025年中国批准其联合化疗用于铂耐药卵巢癌。[22]
16 Firsekibart(金赛药业)
Firsekibart(金赛新®)是一种靶向IL-1β的抗体,用于治疗痛风性关节炎。2025年中国批准该药用于无法耐受NSAIDs或秋水仙碱的患者。临床研究显示,该药可显著减少痛风复发。[23]
17 Trastuzumab botidotin(科伦博泰)
Trastuzumab botidotin(舒泰莱®)是一种HER2靶向ADC,用于治疗HER2阳性乳腺癌。2025年中国批准该药用于既往接受抗HER2治疗后的患者。临床研究显示,该药可显著延长无进展生存期。[24]
18 Becotatug vedotin(乐普生物)
Becotatug vedotin(MEIYOUHENG®)是一种靶向EGFR的ADC,用于治疗复发或转移性鼻咽癌。2025年中国批准该药上市。研究显示,该药相比化疗具有更高的客观缓解率。[25]
19 Picankibart(信达生物)
Picankibart(PECONDLE®)是一种靶向IL-23 p19亚基的抗体,用于治疗中重度斑块型银屑病。2025年中国批准该药上市。[26]
总结
从技术类型来看,2025年获批的抗体药物涵盖多种形式,包括:
- 传统单克隆抗体
- 双特异性抗体
- ADC
从适应症来看,2025年抗体药物不仅继续在肿瘤治疗领域取得进展,同时也在免疫疾病、病毒感染和心血管疾病等领域显示出重要价值。例如,针对 RSV感染、遗传性血管性水肿(HAE)以及IgA肾病等疾病的创新抗体均在2025年获得批准。
总体来看,抗体药物仍然是全球创新药物研发的重要方向。随着抗体工程、ADC技术以及双特异性抗体平台的持续发展,未来几年预计将有更多创新抗体进入临床并获得上市批准。
参考文献
[1] Crescioli S, Reichert JM. Antibodies to Watch in 2026. MAbs. 2026.
[2] Drulyte I, et al. Structural basis for the inhibition of β-FXIIa by garadacimab. Structure. 2024.
[3] InflaRx. European Commission approval for Gohibic (vilobelimab) for treatment of SARS-CoV-2-induced ARDS. 2025.
[4] European Medicines Agency. Gohibic (vilobelimab) product information.
[5] Regeneron Pharmaceuticals. FDA accelerated approval of linvoseltamab for relapsed or refractory multiple myeloma. 2025.
[6] Seth NP, et al. Nipocalimab, an immunoselective FcRn blocker that lowers IgG. MAbs. 2025.
[7] Johnson & Johnson. FDA approval of IMAAVY (nipocalimab) for generalized myasthenia gravis. 2025.
[8] Johnson & Johnson. European Commission approval of nipocalimab for generalized myasthenia gravis. 2025.
[9] U.S. Food and Drug Administration. Accelerated approval of telisotuzumab vedotin for NSCLC with high c-MET expression. 2025.
[10] Merck. FDA approval of Enflonsia (clesrovimab) for prevention of RSV lower respiratory tract disease in infants. 2025.
[11] European Medicines Agency. Enflonsia (clesrovimab) product information.
[12] Otsuka Pharmaceutical. FDA accelerated approval of sibeprenlimab for IgA nephropathy. 2025.
[13] GSK. Depemokimab approved in the UK for asthma and chronic rhinosinusitis with nasal polyps. 2025.
[14] GSK. Positive Phase III ANCHOR trial results for depemokimab. 2024.
[15] Omeros Corporation. FDA approval of YARTEMLEA (narsoplimab) for TA-TMA.
[16] Lamb YN. Recaticimab: first approval. Drugs. 2025.
[17] Patsnap. Finotonlimab: anti-PD-1 antibody for solid tumors. 2025.
[18] Sinocelltech. Finotonlimab approvals for head and neck squamous cell carcinoma and liver cancer indications.
[19] Liang Z, et al. Recombinant monoclonal antibody siltartoxatug for tetanus prevention: a randomized Phase 3 trial. Nature Medicine. 2025.
[20] Akeso. Ebdarokimab approved in China for moderate-to-severe plaque psoriasis. 2025.
[21] Li Z, et al. Trastuzumab rezetecan in HER2-mutant non-small cell lung cancer. Lancet Oncology. 2025.
[22] Simcere Pharmaceutical Group. Approval of Enzeshu (suvemcitug) by the National Medical Products Administration.
[23] Changchun GeneScience. Firsekibart approved for treatment of gouty arthritis.
[24] Kelun-Biotech. Trastuzumab botidotin approved for HER2-positive breast cancer.
[25] Lepu Biopharma. Interim report 2025.
[26] Innovent Biologics. NMPA approval of mazdutide (IBI362) for chronic weight management in adults with obesity or overweight. 2025.
关于康日百奥Bioworkshops
康日百奥Bioworkshops 是一家全球化的生物药合同开发与生产组织(CDMO),专注于抗体类生物药的研发与生产。我们在双特异性、三特异性、融合蛋白等复杂抗体领域具备突出优势,为全球制药与生物技术公司提供从早期研发到商业化生产的一站式解决方案。依托完善的体系和国际标准合规的质量管理,康日百奥Bioworkshops 的服务范围覆盖细胞株构建、工艺开发、原液生产(200L、500L、2000L)、制剂灌装(西林瓶水针、冻干、预充针、卡式瓶等主流剂型,并支持与注射笔等给药装置的配套使用)、工艺表征,工艺验证以及注册申报支持。作为值得信赖的合作伙伴,康日百奥Bioworkshops 已经与来自美国、欧洲、亚太等地的客户开展合作,成功交付其单抗、双抗、多抗、ADC、融合蛋白、细胞因子等项目并获得临床批件。我们坚持以客户需求为中心,通过专业团队和先进平台,加速创新药物的开发和上市进程。
公司业务范围:
细胞株构建 | 细胞培养 | 纯化工艺开发 | 制剂处方开发 | 分析方法开发 | 工艺表征工艺验证 | 原液和成品的 cGMP 生产(200L、500L、2000L) | 无菌灌装(预充针、卡式瓶、注射笔、西林瓶水针、冻干)
















