Bio-Share丨从双抗到多特异性免疫疗法
发布时间: Apr 21 , 2026
近年来,随着肿瘤异质性、免疫逃逸机制以及复杂微环境问题的不断显现,仅依赖两个靶点的调控,已难以支撑更高的治疗需求。于是,多种更具备系统调控能力的分子形式开始出现:TCR双特异性构建体、双特异性适配体、及多特异性免疫疗法[1]。这些技术不仅拥有多靶点协同的特征,还开始了对于免疫反应逻辑的重构。
1. TCR双特异性构建体:从胞内抗原到治疗靶点
长期以来,抗体药物面临着只能识别细胞表面抗原的限制。然而,具有肿瘤特异性的靶点其实来源于细胞内部,例如突变蛋白或异常表达蛋白。这些抗原只有在被加工为抗原肽,并通过MHC分子呈递到细胞表面时,才有可能被免疫系统识别。T细胞受体(TCR)正是负责识别这一抗原肽-MHC复合物的关键分子[2]。基于这样的机制,TCR双特异性构建体被设计且使用:一端负责识别特定的pMHC复合物,另一端则结合T细胞表面的CD3分子,实现对T细胞的激活[3]。TCR双特异性构建体相当于在肿瘤细胞与T细胞之间建立起了功能性桥梁,将免疫杀伤精确地引导至特定靶点,把原本不可药物化的胞内抗原转变为可开发的治疗靶点。
TCR双特异性构建体在实体瘤及免疫治疗领域具有重要的潜力。这项策略的价值不仅在于找到新靶点,更在于推动下一代免疫疗法向更高复杂度的工程体系迈进。
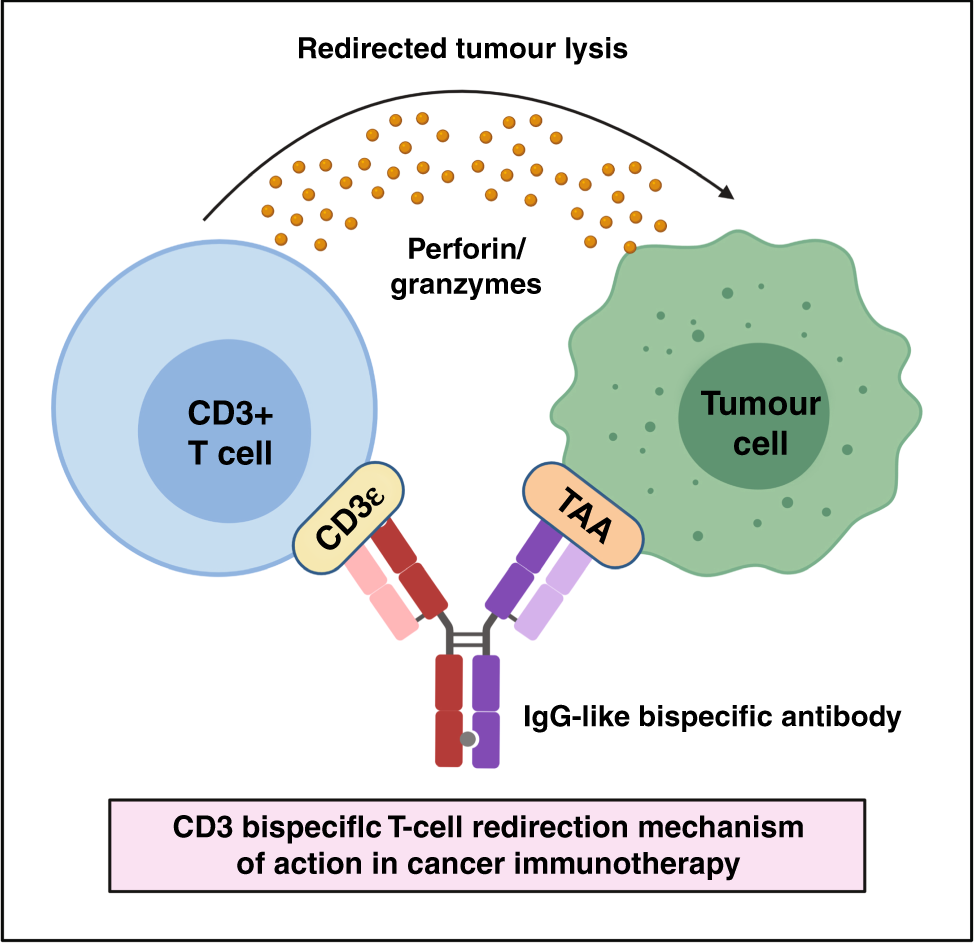
图1:CD3+双特异性T细胞重定向在癌症中的作用机制。来源:Singh, A., Dees, S. & Grewal, I.S. Overcoming the challenges associated with CD3+ T-cell redirection in cancer. Br J Cancer 124, 1037–1048 (2021). https://doi.org/10.1038/s41416-020-01225-5
2. 双特异性适配体:抗体之外的分子形式
如果说TCR双特异性构建体是在拓展靶点范围,那么适配体(aptamer)的发展,则是在对于分子本身来进行思考。适配体是一类由DNA或RNA构成的功能性分子,通过特定的三维折叠结构实现对靶标的高亲和力结合[4]。不同于抗体依赖细胞表达系统,适配体可以通过化学合成获得,这使其在生产一致性与结构可控性方面具有独特优势[5]。
当两个具有不同靶向能力的适配体通过柔性linker连接时,就形成了双特异性适配体。这类分子一端结合免疫细胞,另一端结合靶细胞,从而促进免疫突触的形成[6]。
双特异性适配体不仅关乎于功能替代,更是一种分子层面的革新。更小的分子尺寸代表着更强的组织穿透能力,低免疫原性为长期用药提供潜在优势,而化学合成路径则为结构优化提供了更高自由度[7]。为下一代免疫疗法提供了一种全新的药物形式。
然而,其挑战同样明显。适配体在体内易被核酸酶降解,半衰期较短,并且容易被快速清除[8],这些因素都限制了其体内应用疗效。因此,适配体的开发往往需要结合化学修饰与递送系统进行提高整体的稳定性。
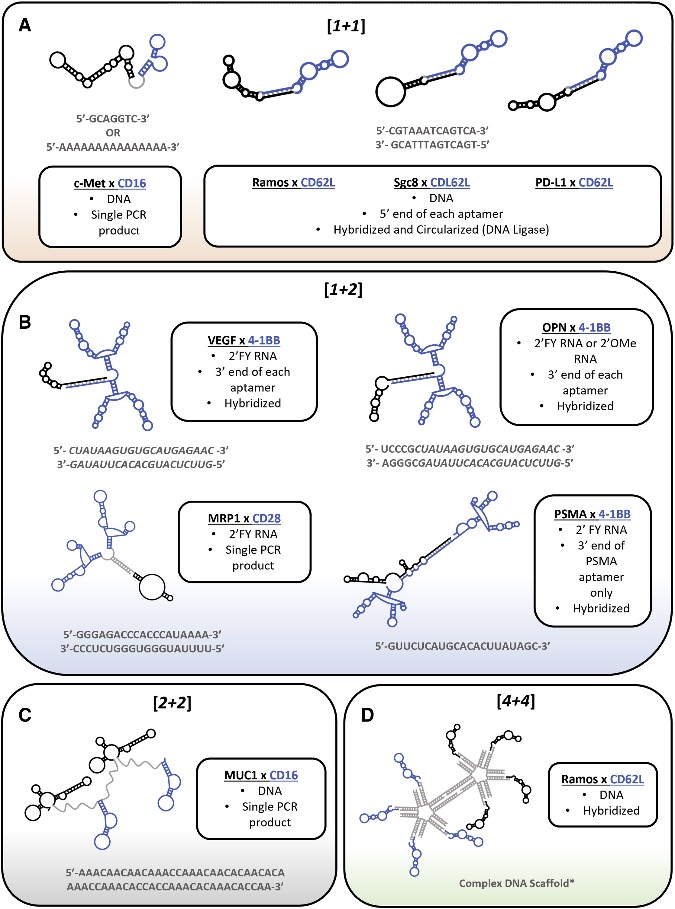
图2:免疫调节双特异性适配体及分类。图中,蓝色部分为靶向免疫细胞的适体,黑色部分为靶向肿瘤的适配体。来源:Thomas B, Porciani D, Burke D Cancer immunomodulation using bispecific aptamers Molecular Therapy Nucleic Acids, 2022; 27, 894-915
3. 多特异性免疫疗法:从双靶点到系统调控
无论是TCR还是适配体,都是基于“双特异性”策略,而免疫系统本身,却是一个高度复杂的网络。因此,未来的核心思考可以侧重于:如何在一个分子中整合多种功能,并对免疫反应进行精细调控。围绕这一目标,多特异性免疫治疗提出了一系列关键策略。
首先,是模块化设计。不同结构域(例如靶向、激活或抑制模块)可以像组件一样进行组合。例如,肿瘤靶向模块与免疫效应激活模块结合到一起,以实现对肿瘤细胞和免疫细胞的同时作用。这种设计不仅有助于灵活地增强特异性,还更容易适配不同疾病场景,提高整体治疗效率 [9]。
其次,不同类型的递送平台可以用于优化多特异性分子的体内分布与稳定性,从而提高安全性并增强治疗效果,并促进其在目标组织中的富集[10]。因此,递送系统的设计与多特异性分子本身的系统调控优化,是相互协同、共同决定治疗效果的关键因素。
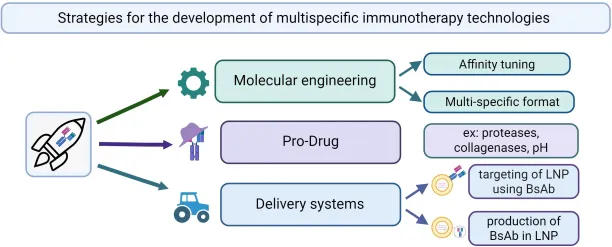
图3:将分子工程策略与递送平台相结合,为多特异性免疫疗法建立了新的范式。来源:Lopatnikova JA and Sennikov SV (2025) Bispecific immunotherapy based on antibodies, T-cell receptors, and aptamers: mechanisms of action, adverse effects, and future perspectives. Front. Immunol. 16:1679092. doi: 10.3389/fimmu.2025.1679092
4. 总结
目前,在双抗的基础之上,新的问题与新的方向应运而生。从TCR到适配体,再到多特异性免疫治疗平台,技术路径正在不断延伸。在这样的背景下,药物研发也正在从传统的分子筛选,逐步转向系统工程与设计。下一代免疫疗法进入了一个更加复杂、也更值得期待的阶段。
参考来源:
[1] Lopatnikova JA and Sennikov SV (2025) Bispecific immunotherapy based on antibodies, T-cell receptors, and aptamers: mechanisms of action, adverse effects, and future perspectives. Front. Immunol. 16:1679092. doi: 10.3389/fimmu.2025.1679092
[2] DahanRReiterY. T-cell-receptor-like antibodies - generation, function and applications. Expert Rev Mol Med. (2012) 14:e6. doi: 10.1017/erm.2012.2
[3] StaegerRTastanovaAGhoshAWinkelbeinerNShuklaPKolmIet al. Tebentafusp elicits on-target cutaneous immune responses driven by cytotoxic T cells in uveal melanoma patients. J Clin Invest. (2025) 135:e181464. doi: 10.1172/JCI181464
[4] EllingtonADSzostakJW. In vitro selection of RNA molecules that bind specific ligands. Nature. (1990) 346:818–22. doi: 10.1038/346818a0
[5] AljohaniMMCialla-MayDPoppJChinnappanRAl-KattanKZourobM. Aptamers: potential diagnostic and therapeutic agents for blood diseases. Molecules. (2022) 27:383. doi: 10.3390/molecules27020383
[6] McNamaraJOKoloniasDPastorFMittlerRSChenLGiangrandePHet al. Multivalent 4-1BB binding aptamers costimulate CD8+ T cells and inhibit tumor growth in mice. J Clin Invest. (2008) 118:376–86. doi: 10.1172/JCI33365
[7] DollinsCMNairSBoczkowskiDLeeJLayzerJMGilboaEet al. Assembling OX40 aptamers on a molecular scaffold to create a receptor-activating aptamer. Chem Biol. (2008) 15:675–82. doi: 10.1016/j.chembiol.2008.05.016
[8] ElskensJPElskensJMMadderA. Chemical modification of aptamers for increased binding affinity in diagnostic applications: current status and future prospects. Int J Mol Sci. (2020) 21:4522. doi: 10.3390/ijms21124522
[9] StaflinKZuch de ZafraCLSchuttLKClarkVZhongFHristopoulosMet al. Target arm affinities determine preclinical efficacy and safety of anti-HER2/CD3 bispecific antibody. JCI Insight. (2020) 5:e133757. doi: 10.1172/jci.insight.133757
[10] FanSHanHYanZLuYHeBZhangQ. Lipid-based nanoparticles for cancer immunotherapy. Med Rev (2021). (2023) 3:230–69. doi: 10.1515/mr-2023-0020
















