Bio-Share | 双特异性抗体三种作用机制解析
发布时间: Apr 14 , 2026
双特异性抗体的作用大致可概括为三类机制:细胞参与(Cell-engagers)、非细胞桥接(Non-cell bridging)、受体-配体阻断(Receptor-ligand blockade)[1]。这三类机制共同构成了双特异性抗体药物设计与功能实现的核心框架。
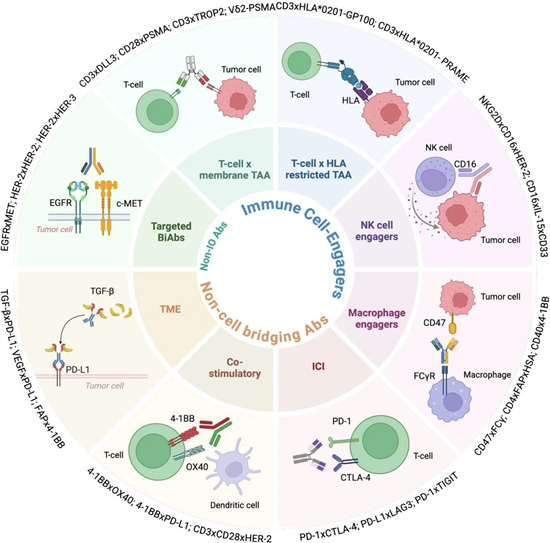
图1:双特异性抗体和多特异性抗体按作用机制分类。来源:Fontana et al., 2026, The Lancet Regional Health – Europe
1、细胞参与疗法(Cell-engaging therapies)
在细胞参与疗法中,T细胞衔接器(TCE)通过物理连接T细胞表面的激活受体(如CD3或NK细胞相关受体),以及肿瘤细胞表面的抗原(如BCMA、CD19等),实现T细胞和癌细胞的桥接,激活T细胞的杀伤功能,释放穿孔素和颗粒酶,直接杀死癌细胞[2]。目前,在血液肿瘤领域,这类机制已经成为代表性的治疗策略。典型TCE主要借助CD3信号激活T细胞,而另一类则通过共刺激受体提供信号2,并协同邻近癌细胞传递信号1。为拓宽靶点范围,研究人员开发了ImmTAC技术,利用高亲和力TCR识别HLA呈递的胞内肽,将多克隆T细胞定向至肿瘤 [3]。
自然杀伤细胞衔接器(NKCE)则通过靶向CD16a、NKG2D等激活受体,调动NK细胞的自身杀伤能力,形成BiKE或TriKE策略 [4]。巨噬细胞衔接器一方面阻断CD47-SIRPα信号,另一方面借助Fcγ受体介导抗体依赖性细胞吞噬(ADCP) [5]。为克服CD47靶向带来的贫血等脱靶毒性,新型双抗策略采用高亲和力结合肿瘤相关抗原、低亲和力结合CD47,同时激活CD40等受体,将巨噬细胞重塑为促炎抗肿瘤表型。
案例:Blinatumomab[6]:
- 靶点:CD3/CD19
- 原理:T细胞通过CD3被拉近肿瘤细胞,形成免疫突触并释放细胞毒因子,实现肿瘤杀伤。
- 临床:Blinatumomab在急性淋巴细胞白血病(ALL)中显著提高完全缓解率,已成为标准免疫治疗药物。
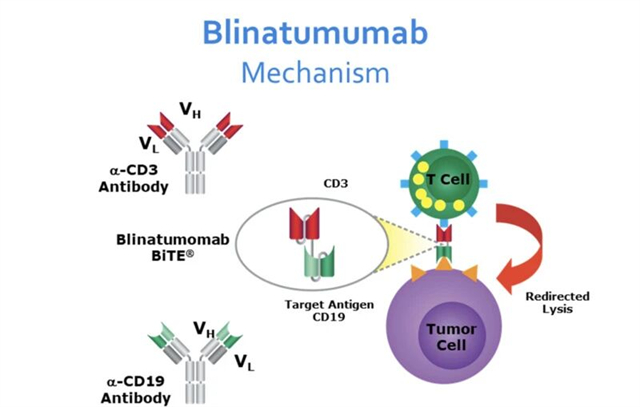
图2:Blinatumumab的作用机制。来源:Chennapragada & Ramadas, 2024, StatPearls, NCBI Bookshelf
2、非细胞桥接疗法(Non-cell bridging therapies)
在非细胞桥接疗法中,双特异性抗体主要通过调控免疫检查点、共刺激信号及肿瘤微环境来增强抗肿瘤免疫。例如,靶向PD-1/CTLA-4等双重免疫检查点抑制剂可产生协同激活效应,帮助克服耐药机制[7]。而共刺激受体激动剂(如OX40/4-1BB)能够提供T细胞完全激活所需的信号2,但存在系统性免疫过度激活的风险[8] 。因此,这一疗法更倾向于采用肿瘤相关抗原限制性组合(如TAA/CD28、TAA/4-1BB)来实现可控的免疫激活[9][10]。
此外,许多肿瘤细胞依赖多条信号通路维持生长增殖和逃避治疗,单靶点抑制容易被旁路激活所抵消。而这类疗法可以同时结合并阻断两条癌细胞生长信号通路(如EGFR/MET),实现协同抑制,从而降低耐药风险,提高疗效。同时,针对肿瘤微环境的双特异性抗体着重逆转免疫抑制状态,代表性药物包括PD-L1/VEGF、TGF-β/PD-L1等,这些组合能够从多个方面解除微环境对免疫应答的束缚[11]。
案例:Amivantamab[12]:
- 靶点:EGFR/MET
- 原理:同时阻断EGFR和MET信号,防止肿瘤通过激活备用通路逃逸。
- 临床:针对EGFR外显子20插入(Exon 20ins)突变型非小细胞肺癌,Amivantamab通过结合受体细胞外结构域突破耐药瓶颈,成为全球首个获批治疗这一特定肺癌亚型的靶向药物。
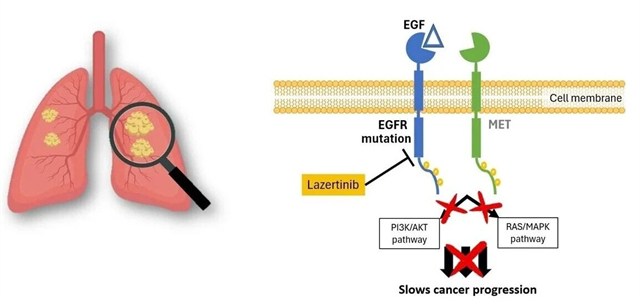
图3:Amivantamab的作用机制。来源:NL Rd1 Tzho,” YouTube video, 2024
3、受体-配体阻断(Receptor-ligand blockade)
在受体-配体阻断策略中,双抗的核心机制是直接干预病理性受体-配体相互作用,阻断信号激活,同时降低组织炎症和血管渗漏。这类双抗可同时抑制多条对肿瘤生长至关重要的信号通路(如EGFR/MET),通过阻断冗余或代偿性通路来克服耐药机制;此外,双位点抗体可以靶向同一受体的两个不同表位(如HER2/HER2)[13],诱导更高效的受体交联、内化及降解,而另一些药物则阻止受体异二聚化(如HER2/HER3),从而阻断下游致癌信号[14]。
在这一策略中,双抗还能同时结合受体和配体,形成稳定的无活性复合物,杀伤肿瘤,使病理信号被彻底抑制。
案例:Faricimab[15]:
- 靶点:VEGF-A/Angiopoietin-2 (Ang-2)
- 原理:VEGF-A促进异常血管生成,Ang-2通过抑制Tie2信号通路,使血管不稳定并加剧炎症反应。Faricimab通过双臂同时抑制VEGF-A和Ang-2,实现抗血管生成、稳定血管结构、抗炎的效果。
- 临床:在黄斑变性和糖尿病性黄斑水肿中,Faricimab展现出更持久的疗效及良好的安全性,大大降低疾病进展风险。
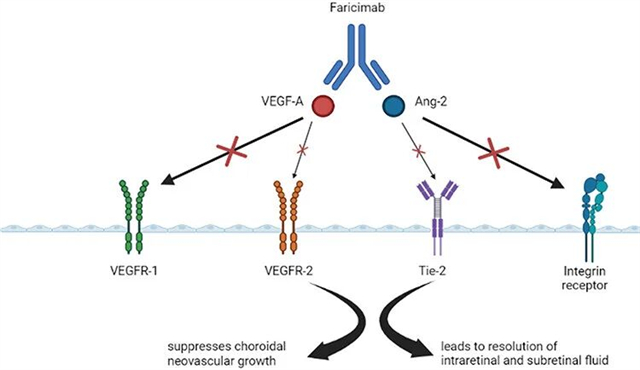
图4:Faricimab的作用机制图。来源:Panos et al., 2023, Drug Design, Development and Therapy
总结
双抗药物通过细胞参与、非细胞桥接、受体-配体阻断三条机制,实现对肿瘤和病理微环境的多维干预。每种机制不仅对应不同的分子设计策略,还与临床应用场景密切相关。从Blinatumomab到Amivantamab,再到Faricimab,这些案例清晰展示了双抗在血液肿瘤及相关疾病中的潜力。随着分子工程和机制理解的进一步深化,未来双抗有望通过多机制融合,实现更高效、更持久的抗肿瘤疗效。
康日百奥Bioworkshops 复杂抗体平台
康日百奥Bioworkshops 拥有成熟的#多特异性抗体开发平台,专注于#复杂抗体开发,平台覆盖双抗、#三抗 等复杂抗体开发的全流程服务:
- 多样化#分子设计 支持:覆盖对称型、非对称型、IgG-like 等多种抗体分子结构,能够在项目早期提供分子设计评估与技术支持,助力高效推进后续工艺开发;
- #高表达系统:优化质粒构建与转染策略,配合高产#稳定细胞株开发,显著提升抗体表达量与正确组装率;
- 完整#开发体系:从#分子设计评估、#细胞株开发、#工艺优化 到#GMP生产,全流程保障双抗等复杂抗体产品的质量与可放大性;
- 成熟项目经验:平台已成功交付多个临床阶段双抗项目,广泛覆盖#肿瘤免疫、#炎症 及#自身免疫 等治疗领域。
关于康日百奥Bioworkshops
康日百奥Bioworkshops 是一家全球化的生物药合同开发与生产组织(CDMO),专注于抗体类生物药的研发与生产。我们在双特异性、三特异性、融合蛋白等复杂抗体领域具备突出优势,为全球制药与生物技术公司提供从早期研发到商业化生产的一站式解决方案。依托完善的体系和国际标准合规的质量管理,康日百奥Bioworkshops 的服务范围覆盖细胞株构建、工艺开发、原液生产(200L、500L、2000L)、制剂灌装(西林瓶水针、冻干、预充针、卡式瓶等主流剂型,并支持与注射笔等给药装置的配套使用)、工艺表征,工艺验证以及注册申报支持。作为值得信赖的合作伙伴,康日百奥Bioworkshops 已经与来自美国、欧洲、亚太等地的客户开展合作,成功交付其单抗、双抗、多抗、ADC、融合蛋白、细胞因子等项目并获得临床批件。我们坚持以客户需求为中心,通过专业团队和先进平台,加速创新药物的开发和上市进程。
公司业务范围:
细胞株构建 | 细胞培养 | 纯化工艺开发 | 制剂处方开发 | 分析方法开发 | 工艺表征工艺验证 | 原液和成品的 cGMP 生产(200L、500L、2000L) | 无菌灌装(预充针、卡式瓶、注射笔、西林瓶水针、冻干)
参考来源:
[1] Elisa Fontana, Rafael Grochot, Nuria Kotecki, Bernard Doger, Simon Nannini, María de Miguel, Evolution of bispecific and multispecific antibodies in cancer therapy,The Lancet Regional Health - Europe, 2026, 101599,
[2] de Miguel M, Umana P, Gomes de Morais AL, Moreno V, Calvo E. T-cell-engaging therapy for solid tumors. Clin Cancer Res. 2021;27(6):1595–1603.
[3] Nathan P, Hassel JC, Rutkowski P, et al. Overall survival benefit with tebentafusp in metastatic uveal melanoma. N Engl J Med. 2021;385(13):1196–1206.
[4] Zhang M, Lam KP, Xu S. Natural Killer Cell Engagers (NKCEs): a new frontier in cancer immunotherapy. Front Immunol. 2023;14: 1207276.
[5] Weiskopf K, Weissman IL. Macrophages are critical effectors of antibody therapies for cancer. MAbs. 2015;7(2):303–310.
[6] “Blinatumomab,” Wikipedia: The Free Encyclopedia, https://en.wikipedia.org/wiki/Blinatumomab
[7] Du Q, Li X, Zhou T, Yang X, Peng F, Han S. 492 development of a tri-specific antibody targeting PD-1/CTLA-4/TIGIT. J Immunother Cancer. 2023;11.
[8] Papadopoulos K, Yap TA, Piha-Paul SA, et al. 1033TiP A first-in-human phase I study of FS120, an OX40/CD137 tetravalent bispecific antibody, in patients with advanced malignancies. Ann Oncol. 2021;32:S864–S865.
[9] Muik A, Garralda E, Altintas I, et al. Preclinical characterization and phase I trial results of a bispecific antibody targeting PD-L1 and 4-1BB (GEN1046) in patients with advanced refractory solid tumors. Cancer Discov. 2022;12(5):1248–1265.
[10] Calvo E, Moreno Garcia V, Oh DY, et al. 40O phase I/Ib open-label study of an HER2-targeted T cell engager (TCE) ÄíSAR443216 in patients (pts) with advanced solid tumors: intravenous (IV) dose-escalation results. ESMO Open. 2025;10:104199.
[11] Wang L, Zhang L, Zhang Z, Wu P, Zhang Y, Chen X. Advances in targeting tumor microenvironment for immunotherapy. Front Immunol. 2024;15:1472772.
[12] “Amivantamab,” Wikipedia: The Free Encyclopedia, https://en.wikipedia.org/wiki/Amivantamab
[13] Zhang J, Ji D, Cai L, et al. First-in-human HER2-targeted bispecific antibody KN026 for the treatment of patients with HER2-positive metastatic breast cancer: results from a phase I study. Clin Cancer Res. 2022;28(4):618–628.
[14] Schram AM, Goto K, Kim DW, et al. Efficacy of Zenocutuzumab in NRG1 fusion-positive cancer. N Engl J Med. 2025;392(6):566–576.
[15] Heier JS, Khanani AM, Quezada Ruiz C, et al. Efficacy, durability, and safety of intravitreal faricimab up to every 16 weeks for neovascular age-related macular degeneration (TENAYA and LUCERNE): two randomised, double-masked, phase 3, non-inferiority trials. Lancet. 2022;399(10326):729–740.
















